Khi con người phát triển kéo theo sự phát triển của các vi khuẩn gây bệnh. Các loại vi khuẩn kháng thuốc cũng ngày càng diễn biến phức tạp hơn đem lại các bất lợi to lớn đối với con người trên toàn thế giới.
Sự ảnh hưởng của các yếu tố mầm mống này đòi hỏi các nhà khoa học tiếp tục nghiên cứu không ngừng nghỉ ra các loại thuốc mới ưu việt hơn các loại thuốc cũ theo tiêu chuẩn chăm sóc nhưng không đạt được kết quả mong muốn bởi sự kháng thuốc ngày càng nghiêm trọng hơn.
Trên khắp thế giới, các nhà nghiên cứu luôn luôn nỗ lực tìm kiếm phương pháp mới nhằm mang lại hiệu quả điều trị tối ưu nhất tới cộng đồng, tận tụy cho sức khỏe cộng đồng loài người trên toàn cầu.
Một trong những nghiên cứu mới nhất về thuốc tiêu diệt và loại bỏ vi khuẩn kháng thuốc H. pylori đã được công bố chính là Talicia®, loại thuốc này đã chính thức được Cục quản lý Thực phẩm và dược phẩm Hoa Kỳ FDA phê duyệt.
Đây là loại thuốc mới mà được rất nhiều người quan tâm bởi nó ảnh hưởng trực tiếp lên sức khỏe con người. Trong bài viết này, https://songkhoe24h.com sẽ cùng bạn tìm hiểu rõ về thông tin này.
Giới thiệu chung về thuốc Talicia và Công ty sản xuất
- RedHill đã có kế hoạch và dự định sẽ ra mắt sản phẩm thuốc Talicia® tại Mỹ vào Q1/2020. Công dụng chính của Talicia® là nhằm điều trị cho những trường hợp bệnh nhân bị nhiễm H. Pylori ở người trưởng thành. Mục tiêu của RedHill chính là chữa trị cho hơn hai triệu bệnh nhân nhiễm H. pylori hằng năm.
- Talicia® lần đầu tiên và duy nhất được FDA phê chuẩn dựa trên nền tảng rifabutin đồng thời nó được tạo ra để giải quyết thực trạng hiện nay, sự kháng thuốc bởi các vi khuẩn ngày càng tăng, khi đó nó làm giảm hiệu quả của tiêu chuẩn chăm sóc dựa trên clarithromycin.
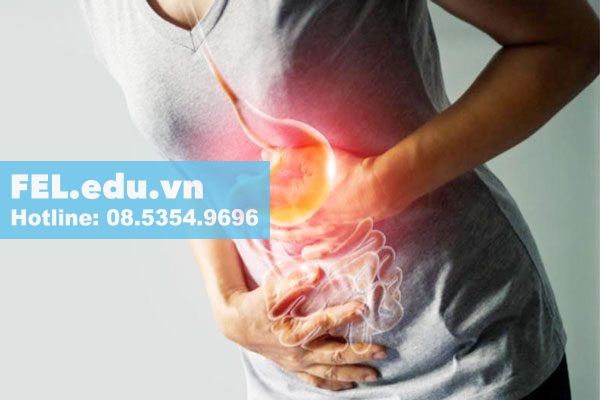
Vi khuẩn H. pylori là tác nhân gây viêm loét dạ dày - Vi khuẩn H. pylori theo thống kê gây ảnh hưởng tới 35% tỉ lệ người trưởng thành ở Hoa Kỳ. Vi khuẩn H. pylori được xếp vào nhóm I của những chất gây ung thư và đây là yếu tố quan trọng tác động lớn nhất tới sự hình thành và phát triển của bệnh loét dạ dày, ung thư dạ dày không gây ra do tim.
- Thuốc Talicia® theo chỉ định của QIDP là đủ điều kiện cho 8 năm độc quyền trên thị trường Hoa Kỳ, ngoại trừ bảo vệ bằng sáng chế kéo dài tới năm 2034.
- Sau các khoản đầu tư chiến lược gần đây của Cosmo Cosmetics, bảng cân đối kế toán không có nợ với các khoản đầu tư ngắn hạn và khoảng 59 triệu dollars tiền mặt.
- Sắp tới, RedHill sẽ tổ chức ngày đầu tư và phân tích đồng thời phát trực tiếp lên trang web vào ngày 22 tháng 11 năm 2019 nhằm giới thiệu kế hoạch ra mắt Talicia® và Aemcolo® và quảng bá rộng rãi sản phẩm này.
TEL-AVIV, Israel và RALEIGH, NC, ngày 4 tháng 11 năm 2019, RedHill Biopharma Ltd. Công ty RedHill hay có tên gọi là Công ty dược phẩm sinh học, đây là một Công ty Dược phẩm sinh học tập trung đặc biệt vào sự phát triển và thương mại hóa cho các loại thuốc độc quyền có tác dụng điều trị các bệnh về đường tiêu hóa.
Đã có thông báo chính thức, Cục quản lý Thực phẩm và Dược phẩm Hoa Kỳ (FDA) đã phê duyệt Talicia®.
Loại thuốc bào chế dạng viên nang giải phóng chậm, hàm lượng khác nhau như 10mg/250mg/12,5mg nhằm điều trị các trường hợp bệnh nhân nhiễm vi khuẩn H. pylori ở người trưởng thành. RedHill dự kiến sẽ ra mắt sản phẩm này vào quý một năm 2020 cùng với nguồn nhân lực bán hàng có dày dặn chuyên môn và có kiến thức về loại thuốc này nhằm hỗ trợ tư vấn cho người sử dụng.
Công ty RedHill đã quảng bá nhiều sản phẩm chữa trị đường tiêu hóa tại Mỹ. Aemcolo và Talicia là hai sản phẩm được dự kiến ra mắt tại Hoa Kỳ trong năm 2019.
Các giai đoạn và quá trình lâm sàng cuối cùng vô cùng quan trọng của Talicia trước khi chính thức đưa ra thị trường bao gồm:
- Kết quả khả quan từ các nghiên cứu với bệnh Crohn
- Các nghiên cứu pivotal đã được lên kế hoạch đối với nhiễm trùng Mycobacteria mà không gây nhiễm khuẩn phổi
- Kết quả dương tính từ nghiên cứu cho viêm dạ dày ruột cấp tính, viêm dạ dày.
- Thiên về nghiên cứu nhiều về bệnh ung t
Talicia® dựa trên nền tảng rifabutin để điều trị cho các trường hợp nhiễm trùng H. pylori hư, đường tiêu hóa và ung thư đường mật.
Bên cạnh đó còn có thêm các quy trình khác.
Talicia® là phương pháp điều trị duy nhất dựa trên nền tảng rifabutin để điều trị cho các trường hợp nhiễm trùng H. pylori. Sản phẩm được thiết kế theo tiêu chuẩn chăm sóc điều trị clarithromycin đang hiện hành để giải quyết sự kháng lại của vi khuẩn H. pylori.
Người ta ước tính rằng, sự kháng lại của vi khuẩn H. pylori với clarithromycin đã tăng gấp đôi trong giai đoạn những năm 2009-2013.
RedHill dự định tổ chức Nhà đầu tư và Phân tích diễn ra vào ngày 22 tháng 11 năm 2019 tại New York để xem xét các kế hoạch ra mắt sản phẩm mới này cũng như cung cấp các hoạt động thương mại một cách tổng quan. Công ty sẽ cung cấp một webcast trực tiếp sự kiện này website của công ty cùng với các thông in đi kèm khác.
Về Talicia®
Talicia® ( omeprazole magiê, amoxicillin và rifabutin), là viên nang giải phóng chậm 10mg/250mg/12,5mg, chúng sử dụng với liều cố định. Thuốc Talicia là sự kết hợp của hai loại kháng sinh amoxicillin và rifabutin và chất omeprazole có tác dụng ức chế bơm proton (PPI).
Thành phần của Talicia bao gồm:
- Omeprazole (một chất ức chế bơm proton hoạt động)
- Amoxicillin (dùng để kháng khuẩn nhóm penicillin)
- Rifabutin (một loại kháng sinh rifamycin)
Talicia đã được FDA phê chuẩn nhằm điều trị bệnh cho các trường hợp nhiễm vi khuẩn H. pylori ở người trưởng thành.
Để giảm thiểu sự phát triển và sinh sôi của các loại vi khuẩn kháng thuốc đồng thời duy trì hiệu quả của Talicia cùng các loại thuốc kháng khuẩn khác, các chuyên gia khuyến cáo Talicia chỉ nên sử dụng nhằm mục đích điều trị hoặc ngăn ngừa sự nhiễm trùng mà đã được xác định rõ hoặc nghi ngờ khả năng cao là do vi khuẩn.
Talicia được tạo ra nhằm giải quyết vấn đề kháng thuốc ngày càng gia tăng mà nguyên nhân là do vi khuẩn H. pylori. Các vi khuẩn này đã kháng lại các loại thuốc kháng sinh thông thường đã từng áp dụng theo các liệu pháp tiêu chuẩn hiện hành. Điều này đã khiến các nhà nghiên cứu phải tìm ra các phương pháp điều trị mới, ở đây chính là Talicia.
Sự chấp thuận của FDA đối với Talicia dựa trên kết quả của hai nghiên cứu ở Mỹ để điều trị cho bệnh nhân trưởng thành nhiễm vi khuẩn H. pylori. Các trường hợp này nói ra các biểu hiện của họ là đau thượng vị và khó chịu ở khu vực này.
Nghiên cứu giai đoạn 3 kiểm chứng Talicia đã chứng minh được rằng khả năng loại trừ vi khuẩn H pylori ở Talicia chiếm tới 84%. Thêm nữa, người ta nhận ra rằng các trường hợp có nồng độ thuốc trong máu được đo vào ngày thứ 13 có tỷ lệ 90,3% đáp ứng ở nhóm sử dụng Talicia so với 64,7% nhóm hoạt động không có kháng với rifabutin-một thành phần chính của Talicia.

Các thống kê cho thấy rằng, 1% bệnh nhân đã ngừng điều trị Talicia do các phản ứng bất lợi trong thuốc gây nên. Các triệu chứng bất lợi hay nói cách khác chính là các tác dụng phụ thường gặp khi sử dụng Talicia mà người bệnh gặp phải như buồn nôn và nôn, ngạt mũi và viêm mũi họng.
Talicia đủ điều kiện cho 8 năm độc quyền thị trường Hoa Kỳ theo chỉ định của QIDP, ngoại trừ việc bảo vệ bằng sáng chế kéo dài tới ít nhất là năm 2034.
Về H. pylori
Hơn 50% dân số thế giới có thể chịu ảnh hưởng của vi khuẩn H. pylori và hơn 35%, tức là khoảng hơn 100 triệu dân số trưởng thành ở Hoa Kỳ.
Con số 2,5 triệu bệnh nhân tiếp nhận điều trị hằng năm ở Hoa Kỳ đã khiến cho vi khuẩn H. pylori được xếp vào những chất gây ung thư nhóm I theo Cơ quan Nghiên cứu Ung thư Quốc tế. Đây là yếu tố, là nguy cơ lớn nhất, tác động mạnh nhất tới sự hình thành và phát triển các tế bào ung thư dạ dày và là nguyên nhân quan trọng nhất dẫn tới bệnh loét dạ dày và loét niêm mạc dạ dày liên quan tới mô lymphoid (MALT), u lympho.
Với những trường hợp bệnh nhân nhiễm bệnh sẽ có nguy cơ cao gấp 6 lần những người khác về sự phát triển phi ung thư dạ dày cardia và u lympho MALT.
Quá trình tiêu diệt và loại bỏ vi khuẩn H. pylori ngày càng trở nên khó khăn khi mà thực tế đã chứng minh rằng, các tiêu chuẩn chăm sóc hiện nay đã thất bại lên tới 25-40%. Đây là số lượng phần trăm bệnh nhân vẫn còn dương tính với H. pylori, nguyên nhân là sự kháng H. pylori với clarithromycin và metronidazole trong các loại kháng sinh thông thường.
Loại vi khuẩn H. pylori kháng Clarithromycin đã được tổ chức y tế thế giới WHO chính thức xếp chúng vào loại mầm bệnh cần phải ưu tiên cao nhằm nghiên cứu, phát triển để tìm ra các phương pháp điều trị mới đặc hiệu cho loại mầm bệnh nguy hiểm này.
Chỉ định và sử dụng
Chỉ định: Điều trị các trường hợp nhiễm H. pylori ở người trưởng thành.
Để hạn chế sự phát triển của vi khuẩn kháng thuốc cũng như duy trì hiệu quả của Talicia và các loại thuốc kháng khuẩn khác, Talicia được khuyên chỉ nên dùng để điều trị và ngăn ngừa khả năng nhiễm trùng mà người sử dụng đã được chẩn đoán hoặc nghi ngờ cao do nhiễm vi khuẩn gây ra.
Chống chỉ định
- Không dùng cho các trường hợp quá mẫn cảm với các thành phần của thuốc Talicia hoặc bất kỳ một loại thuốc kháng khuẩn beta-lactam nào.
- Các sản phẩm chứa Rilpivirine
- Delavirdine
- Voriconazole
- Gây ảnh hưởng bất lợi tới thai nhi
- Không dùng cho các bệnh nhân suy thận nặng
- Không dùng cho các trường hợp suy gan.
Cảnh báo và đề phòng
- Cẩn trọng với các trường hợp quá mẫn cảm với các thành phần trong thuốc cũng như mẫn cảm với các loại thuốc kháng khuẩn. Phản ứng nguy hiểm có thẻ gây sốc phản vệ hoặc gây tử vong. Các trường hợp như vậy được báo cáo về thành phần có trong Talicia. Nếu có các phản ứng quá mẫn, hãy ngừng sử dụng Talicia và điều trị khắc phục ngay lập tức, tránh các sự cố đáng tiếc xảy ra.
- Có thể có trường hợp bị tiêu chảy, đã có báo cáo sơ bộ về trường hợp này.
- Tác dụng của Talicia có thể làm giảm hiệu quả đối với thuốc tránh thai hay các thuốc nội tiết tố khác. Các chuyên gia khuyên rằng không sử dụng các biện pháp tránh thai mà thành phần của nó có bổ sung thành phần nội tiết tố khi đang sử dụng Talicia để điều trị nhiễm khuẩn H. pylori. Nếu quan hệ không mong muốn có thai, hãy sử dụng các biện pháp tránh thai không nội tiết tố như bao cao su, vòng tránh thai…
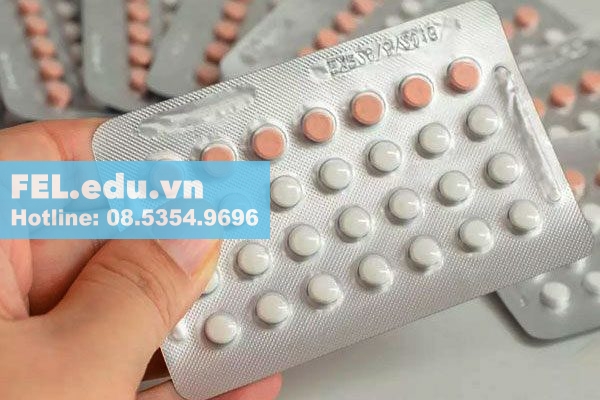
Talicia® làm giảm tác dụng của các loại thuốc tránh thai - Các trường hợp sử dụng Talicia có nguy cơ dẫn tới viêm thận cấp tính (AIN) hay có thể do dùng thuốc có chứa hàm lượng penicillin hay các hoạt chất ức chế sự hoạt động của bơm proton. Bệnh nhân ngừng sử dụng khi có biểu hiện bất thường liên quan tới viêm thận xayra.
- Có thể bị lupus ban đỏ và toàn thân. Chủ yếu xảy ra ở da. Đây có thể là khởi đầu cho một mầm bệnh mới hoặc đã làm bệnh tình trở nên trầm trọng hơn. Hãy ngưng sử dụng Talicia khi có những triệu chứng bất thường này.
Tác dụng phụ
Khi sử dụng Talicia, bệnh nhân có thể có các tác dụng phụ như:
- Đau bụng, tiêu chảy: đây là tác dụng phụ được cho là phổ biến nhất
- Nhức đầu, buồn nôn và nôn
- Khó tiêu
- Phát ban đỏ
- Đau họng, viêm họng
- Nhiễm nấm Candida ở âm hộ ( đối với phụ nữ)
Tương tác thuốc
Talicia có chứa những thành phần có khả năng tương tác với các chất trong thuốc khác hoặc sản phẩm khác mà đã được tiến hành thử nghiệm trên lâm sàng.
Bệnh nhân nên xem thêm các thông tin đầy đủ về tương tác thuốc với Talicia trong đơn.
Các ý kiến từ các giáo sư và người đứng đầu sản xuất
Giáo sư David Y. Graham, Giáo sư Y học, Virus học và Vi sinh học phân tử tại Đại học Y Baylor, Houston đồng thời là Trưởng nhóm nghiên cứu của Talicia® giai đoạn 3, cho rằng: Talicia® là một phương pháp điều trị mới và cần thiết cho vi khuẩn H. pylori mà bệnh nhân có thể lựa chọn. Đây là phương pháp không những an toàn mà còn đem lại hiệu quả tuyệt vời mà không gây tổn thương bởi kháng Clarithromycin hay Metronidazole. Các nghiên cứu lâm sàng về Talicia® đã chứng minh được hiệu quả của thuốc trong quá trình tiêu diệt vi khuẩn H. pylori. Các nghiên cứu đã đưa ra con số 17% những trường hợp kháng clarithromycin và hầu hết không kháng rifabutin. Như vậy thấy rằng nó phù hợp với dữ liệu hiện tại và chứng minh các liệu pháp chứa clarithromycin thất bại trong khoảng 2540% các trường hợp.

Colin W. Howden, Hyman, ông là Giáo sư Y khoa và là Trưởng Bộ phận của Gastroenterology, Đại học Trung tâm Khoa học Y tế Tennessee cung cấp thêm: Vi khuẩn H. pylori là một trong các nguyên nhân chính gây ra viêm loét dạ dày đồng thời gây ra bệnh ung thư. Đây là loại vi khuẩn được xếp vào các nguy cơ hàng đầu gây ung thư dạ dày. Quá trình điều trị bệnh do nhiễm vi khuẩn này ngày càng trở nên khó khăn do thực tế, sự kháng vi khuẩn đang tiếp diễn theo chiều hướng gia tăng và phức tạp hơn cùng với đó trong những thập kỷ qua, các công nghệ hiện đại áp dụng vào chữa trị bệnh vẫn còn thiếu thốn. Như vậy, việc nghiên cứu ra sẽ là bước ngoặt mới ưu việt hơn và hiệu quả cao hơn, tối ưu hơn so với các phương pháp cũ. Ông tin rằng đây sẽ trở thành phương pháp điều trị theo tiêu chuẩn hàng đầu được đề nghị lựa chọn đối với các trường hợp bệnh nhân nhiễm H. pylori.
Ông Dror Ben-Asher, Giám đốc điều hành của RedHill Biopharma cho biết: sự phê duyệt và chấp thuận của FDA về Talicia® đã minh chứng cho sự cống hiến to lớn không ngừng nghỉ của những người nghiên cứu dành cho những bệnh nhân không may mắc phải các bệnh về đường tiêu hóa. Chúng tôi rất cảm ơn những nhà nghiên cứu, những nhân viên lâm sàng và các bệnh nhân đã tham gia trong suốt quá trình nghiên cứu ra Talicia và nhóm RedHill cùng những nhà tài trợ đã cung cấp để có được cột mốc to lớn vĩ đại này. Nó đạt được bởi sự cam kết, quyết tâm và quá trình làm việc bền bỉ tận lực của họ. Chúng tôi đang nỗ lực mở rộng quy mô về nhân lực bán hàng của mình lên trên khoảng 140 triệu đại diện, đó là những người sẽ quảng bá về Talicia và Aemcolo cũng như các sản phẩm tập trung cao vào điều trị các vấn đề về đường tiêu hóa đang có trong giỏ hàng của công ty.
Các thông tin trên đây đều mang định hướng tương lai từ nhà sản xuất, sản phẩm Talicia đang trên những giai đoạn kiểm nghiệm lâm sàng cuối cùng trước khi chính thức đưa vào thị trường và điều trị cho các bệnh nhân nhiễm vi khuẩn H. pylori.
Sản phẩm thuốc Talicia còn những giả định nhất định về các tác dụng và rủi ro của thuốc sau khi sử dụng, những điều đã biết hoặc chưa tìm ra mà nằm ngoài tầm kiểm soát của Công ty mà công ty chưa thể dự đoán trước được.
Kết quả lâm sàng thử nghiệm và kết quả thực tế sau khi đưa vào sử dụng có thể khác nhau. Những rủi ro ở đây được nhắc tới là không giới hạn. Nó bao gồm nhiều khía cạnh như thời điểm chính thức ra mắt và đưa sản phẩm vào thực tế tới người bệnh, quá trình hoàn thành, khởi điểm, tốc độ tiến trình của thuốc, các thí nghiệm tiền lâm sàng, lâm sàng, thời gian nộp hồ sơ, thời gian nghiên cứu bổ sung, nhận phê duyệt… và các vấn đề liên quan tới lĩnh vực kinh tế như sản xuất, thương mại hóa và khả năng lưu thông thương mại…

Trước khi chính thức đưa ra sản phẩm mới nào, trong đó cụ thể như thuốc Talicia thì đứng tên là một công ty, RedHill cũng cần phải có các thủ tục liên quan, các chứng chỉ phê duyệt thuốc, cấp phép lưu hành. Ngoài ra còn cần có các ước tính chi phí, nguồn vốn đầu vào đầu ra, các trải nghiệm của người dùng và thống kê sau khi phát hành thuốc để kiểm tra thực tế tác dụng của thuốc đối với thực tiễn người sử dụng.
Tài liệu tham khảo:
- RedHill Biopharma Announces FDA Approval of Talicia® for Treatment of H. pylori in Adults. Link:
https://www.redhillbio.com/RedHill/Templates/showpage.asp?DBID=1&LNGID=1&TMID=178&FID=1395&PID=0&IID=13236




